Phương pháp PCR được thực hiện theo quy trình như thế nào để chẩn đoán được bệnh ung khí thán ở trâu?
Phương pháp PCR dùng để chẩn đoán bệnh ung khí thán ở trâu cần sử dụng cặp mồi nào?
Theo tiết 5.2.4.3 tiểu mục 5.2 Mục 5 Tiêu Tiêu chuẩn quốc gia TCVN 8400-23:2014 về Bệnh động vật - Quy trình chẩn đoán - Phần 23: Bệnh ung khí thán quy định về cách xác định vi khuẩn bằng phương pháp PCR như sau:
Cách tiến hành
...
5.2. Chẩn đoán trong phòng thí nghiệm
...
5.2.4.3. Xác định vi khuẩn Clostridium chauvoei bằng phương pháp PCR (Polymerase Chain Reaction)
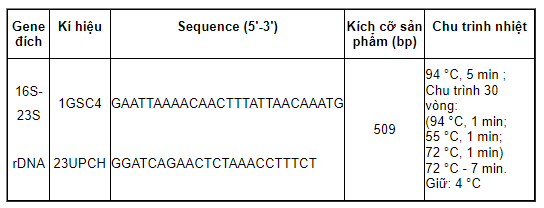
Sử dụng phương pháp PCR với cặp mồi đặc hiệu và chu trình nhiệt ở Bảng 2.
Bảng 2 - Cặp mồi và chu trình nhiệt cho PCR
Tiến hành phản ứng PCR theo Phụ lục C.
Theo đó, để tiến hành phương pháp PCR cần sử dụng cặp mồi theo tiêu chuẩn nêu trên.
Nguyên liệu cần thiết cho phương pháp PCR để chẩn đoán bệnh ung khí thán ở trâu là gì?
Theo điểm C.1 Phục lục C ban hành kèm theo Tiêu chuẩn quốc gia TCVN 8400-23:2014 về Bệnh động vật - Quy trình chẩn đoán - Phần 23: Bệnh ung khí thán quy định về nguyên liệu dùng cho phương pháp PCR gòm:
- Taq PCR Master Mix Kit.
- Cặp mồi (primers): mồi xuôi và mồi ngược (Bảng 2).
- Nước tinh khiết không có nuclease.
- Dung dịch đệm TAE hoặc TBE.
- Chất nhuộm màu Ethidi bromua hoặc SYBR green.
- Loading dye.
- DNA chuẩn (Ladder, marker).
Phương pháp PCR được thực hiện theo quy trình như thế nào để chẩn đoán được bệnh ung khí thán ở trâu?

Phương pháp PCR được thực hiện theo quy trình như thế nào để chẩn đoán được bệnh ung khí thán ở trâu? (Hình từ Internet)
Theo điểm C.1, C.2, C.4 và điểm C.4 Phục lục C ban hành kèm theo Tiêu chuẩn quốc gia TCVN 8400-23:2014 về Bệnh động vật - Quy trình chẩn đoán - Phần 23: Bệnh ung khí thán quy định về các bước tiến hành phương pháp PCR như sau:
PHỤ LỤC C
(Qui định)
Phát hiện vi khuẩn Clostridium chauvoei bằng phương pháp PCR
....
C.2. Chuẩn bị mẫu
Mẫu kiểm tra là vi khuẩn nghi là Clostridium chauvoei được cấy trên thạch máu (xem 3.1) và nuôi trong tủ ấm (xem 4.1) ở điều kiện yếm khí trong 48 h.
Đối chứng dương: Chủng vi khuẩn đã được giám định là Clostridium chauvoei hoặc sử dụng các chủng Clostridium chauvoei chuẩn.
C.3. Tách chiết DNA
Các vi khuẩn phân lập được từ mẫu bệnh phẩm, các mẫu đối chứng dương được tách chiết DNA bằng các kit thương mại và tiến hành các bước theo chỉ dẫn của nhà sản xuất.
C.4. Phản ứng PCR
Sử dụng cặp mồi (primer) và chu trình nhiệt trong Bảng 2 và chuẩn bị mồi ở nồng độ 20 μM. Hỗn hợp phản ứng được chuẩn bị trong ống 0,2 ml. Thành phần cho 1 phản ứng (theo hướng dẫn của Kit Taq PCR master mix Kit-Qiagen) như sau:
- Taq PCR Master Mix Kit 12,5 μl
- Mồi xuôi 20 μl 1 μl
- Mồi ngược 20 μl 1 μl
- Nước không có nuclease 8.5 μl
- Mẫu DNA 2 μl
Tổng thể tích 25 μl
Đối chứng dương: DNA tách chiết từ vi khuẩn Clostridium chauvoei (xem C.2).
Đối chứng âm: Gồm đầy đủ thành phần của một phản ứng PCR, nhưng không có DNA của vi khuẩn.
C.5. Chạy điện di
Sản phẩm PCR được chạy điện di trên thạch agarose từ 1,5 % đến 2 % trong dung dịch đệm TAE hoặc TBE.
Cho 2 μl dung dịch loading dye vào 8 μl sản phẩm PCR, trộn đều cho vào từng giếng trên bản thạch. Cho 10 μl thang chuẩn (marker) vào một giếng.
Bản thạch được điện di trong môi trường dung dịch đệm TAE hoặc TBE (tùy thuộc vào loại đệm sử dụng khi pha thạch), trong thời gian từ 30 min đến 40 min, ở 100 V, sau đó nhuộm bản thạch (sản phẩm PCR) bằng dung dịch ethidium bromide 0,2 mg/100 ml.
Có thể dùng chất nhuộm màu khác như SYBR green để nhuộm bản thạch (sản phẩm PCR) và sử dụng theo qui định của nhà sản xuất (ví dụ: SYBR sate DNA gel stain của Invitrogen).
C.6. Đọc kết quả
Phản ứng dương tính khi:
- Mẫu đối chứng dương: Có một vạch duy nhất đúng kích cỡ của sản phẩm;
- Mẫu đối chứng âm: Không xuất hiện vạch;
- Mẫu kiểm tra: Có vạch giống mẫu đối chứng dương.
Phản ứng âm tính khi:
- Mẫu đối chứng dương: Có một vạch duy nhất đúng kích cỡ của sản phẩm;
- Mẫu đối chứng âm: Không xuất hiện vạch;
- Mẫu kiểm tra: Không xuất hiện vạch;
Cần chuẩn bị mẫu kiểm tra là vi khuẩn nghi là Clostridium chauvoei được cấy trên thạch máu và nuôi trong tủ ấm ở điều kiện yếm khí trong 48 h.
Các vi khuẩn phân lập được từ mẫu bệnh phẩm, các mẫu đối chứng dương được tách chiết DNA bằng các kit thương mại và tiến hành các bước theo chỉ dẫn của nhà sản xuất.
Sử dụng cặp mồi (primer) và chu trình nhiệt trong Bảng 2 và chuẩn bị mồi ở nồng độ 20 μM. Hỗn hợp phản ứng được chuẩn bị trong ống 0,2 ml.
Sản phẩm PCR được chạy điện di trên thạch agarose từ 1,5 % đến 2 % trong dung dịch đệm TAE hoặc TBE. Cho 2 μl dung dịch loading dye vào 8 μl sản phẩm PCR, trộn đều cho vào từng giếng trên bản thạch. Cho 10 μl thang chuẩn (marker) vào một giếng.
Sau đó thực hiện chay điện di sản phẩm PCR trên thạch agarose từ 1,5 % đến 2 % trong dung dịch đệm TAE hoặc TBE. Cho 2 μl dung dịch loading dye vào 8 μl sản phẩm PCR, trộn đều cho vào từng giếng trên bản thạch. Cho 10 μl thang chuẩn (marker) vào một giếng.
Bản thạch được điện di trong môi trường dung dịch đệm TAE hoặc TBE (tùy thuộc vào loại đệm sử dụng khi pha thạch), trong thời gian từ 30 min đến 40 min, ở 100 V, sau đó nhuộm bản thạch (sản phẩm PCR) bằng dung dịch ethidium bromide 0,2 mg/100 ml. Cuối cùng thực hiện đọc kết quả phản ứng.
Quý khách cần hỏi thêm thông tin về có thể đặt câu hỏi tại đây.